به گفته Andro von eschenbach، سرپرست انستيتو ملي سرطان، فناورينانو، دانش مربوط به مقياسهاي کوچک، در حال جذب بزرگترين دانشمندان از سراسر دنيا در زمينههاي گوناگون علمي و مهندسي ميباشد و هدف آن معطوف و هماهنگ كردن استعدادها و ذهن آنها بر روي حل مسائل و مشکلاتي است که بر سر راه تحقيقات در مورد تجهيزات درمان باليني وجود دارد. به عقيده وي، نانومواد و نانوابزارها نقشي بينظير و حياتي را در تبديل دانش به پيشرفتهاي مفيد باليني در زمينه تشخيص و درمان سلولهاي سرطاني ايفا ميکنند، كاري که با انجام آن روند تشخيص و درمان و نهايتاَ پيشگيري از سرطان کاملاَ متحول خواهد شد.مثالي که ميتواند به منظور درک بيشتر پتانسيل وسيع فناورينانو در زمينه تغيير روشهاي تشخيص و درمان سرطان به کار رود استفاده از نانوذرات ميباشد.
استفاده از نقاط کوانتومي در تشخيص و درمان سرطان
استفاده از نقاط کوانتومي به عنوان ابزارهاي جديد تشخيص سرطان در مراحل اوليه، بسيار نويدبخش بوده است، اما وجود نگرانيها درباره اثرات سمي اين ذرات روي بدن، توسعه باليني آنها را محدود کرده است. محققان دانشگاه بوفالو روش جديدي براي ساخت نقاط کوانتومي توسعه دادهاند که شايد بتواند اين محدوديت را از بين ببرد. اين کشف آنها درست سر موقع اتفاق افتاده است، زيرا گروهي ديگر از محققان در دانشگاه تگزاس واقع در آرلينگتون (UTA) نشان دادهاند که نقاط کوانتومي ميتوانند به عنوان دماسنجهاي نانومقياس عمل کرده و درمانهاي حرارتي مختلف مبتني بر نانوذرات را که براي درمان سرطان توسعه يافتهاند، راهنمايي کنند.

دکتر پاراس پراساد از دانشگاه بوفالو روي روشهاي مختلف توليد نقاط کوانتومي جديد کار کرده است. آخرين کار وي که در مجله Small منتشر شده است، منجر به توليد نقاط کوانتومي زيستسازگاري شده که تا بيش از سه ماه پس از تزريق هيچ اثر سميتي از خود نشان نميدهند. اين نقاط کوانتومي داراي يک هسته از جنس سولفيد کادميوم هستند که با لايه نازکي از کادميوم، سلنيوم و تلوريوم پوشانده شدهاند. آنها نقاط توليد شده را با يک لايه زبر از يک ماده آبگريز روکشدهي کرده و بدين ترتيب از نشت اين فلزات سمي به درون بدن جلوگيري نمودند. اين روکش همچنين داراي گروههاي شيميايي است که ميتوان عوامل هدفگير يا داروها را به آنها متصل کرد.
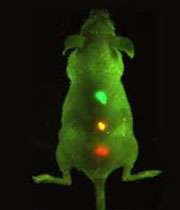
دکتر پراساد و همکارانش توانستند پس از تزريق اين ذرات بسيار درخشنده به بدن موش، با استفاده از طيفسنجي مادون قرمز نزديک از آنها تصويربرداري کرده و محل تجمع آنها را درون بدن تشخيص دهند. بر خلاف نقاط کوانتومي معمول، احتمال تجمع اين ذرات روکشدهي شده در کبد و طحال پايين است. مطالعه بافتهاي جداشده از بدن موش 100 روز پس از تزريق نشان داد که هيچ گونه آسيب ناشي از تجمع نقاط کوانتومي در آنها ديده نميشود. اين پژوهشگران همچنين گزارش نمودهاند موشهايي که تزريق روي آنها صورت گرفته بود، در طول دوره مطالعه رفتار عادي از خود نشان ميدادند.
در همين حال، دکتر بوسمو هان از UTA در مقاله منتشر شده درAnnals of Biomedical Engineering گزارش کرده که توانسته است از نقاط کوانتومي تلوريد کادميوم/سولفيد روي به عنوان دماسنجهاي نانومقياسي که ميتوانند تغييرات دماي موضعي را به صورت بلادرنگ تشخيص دهند، استفاده کند. هدف از انجام اين کار ايجاد يک ابزار تشخيصي است که تومورشناسان را قادر ميسازد رسيدن به دماي مناسب براي کشتن سلولها در فرايند حرارتدرماني را تشخيص دهند.
ترکيب اين دو کار پژوهشي ميتواند براي تشخيص و درمان کاراتر سرطان در آينده نويدبخش باشد.
استفاده از نانوذرات مغناطيسي در درمان سرطان
افزايش دماي بافتهاي بدن انسان تا بيش از 5 درجه سيلسيوس مي تواند تمام فعاليتهاي عادي سلولي را متوقف و منجر به مرگ سلولها شود که به اين روش، درمان انهدام حرارتي ميگويند. چندين گروه از محققان در حال گسترش نانوذرات و نانولولههاي كربني به عنوان گرمكنندههاي نانومقياس براي استفاده در درمان سرطان هستند و نشان دادهاند استفاده از نانوذرات مغناطيسي و گرم کردن آنها با اعمال ميدان مغناطيسي متناوب ميتواند در انهدام تومورها مفيد واقع شود.
گروهي از محققان از موسسة Triton Biosystem و دانشگاه كاليفرنيا نشان دادند كه ذرات مغناطيسي اكسيدآهن كه به يك پادتن متصل ميشوند، قادرند مولكولهاي سرطاني را تشخيص داده، از جريان خون خارج و به سلولهاي تومور هدف، متصل شوند. اين محققان از يك پادتن نشاندار با عنصر راديواكتيو اينديم– III استفاده كردند و توانستند اتصال اين ذرات به سلولهاي سرطاني سين? موش را تشخيص دهند.
توانايي رديابي اين نانوذرات، پژوهشگران را قادر ميسازد تا زمان بهينه شروع درمان حرارتي را تعيين كنند. اعمال ميدان مغناطيسي متناوب در اين زمان منجر به كاهش چشمگير اندازة تومور ميشود.همچنين اين محققان در مقاله ديگري نشان دادند که ميتوانند براي گرم كردن نانوذرات جهت انهدام سلولهاي سرطاني جانواران بدون آسيب به سلولهاي سالم، از ميدانهاي مغناطيسي متناوب با دامنة بالا استفاده کند. اساس استفاده از اين ميدانها پالسيكردن ميدانها با فركانس مناسب است، به گونهاي كه بافتهايي كه نانوذرات در آنها تجمع نكردهاند گرم نشوند. با استفاده از ميدان مغناطيسي پالسي هيچ گونه عوارض جانبي درموشهاي آزمايشي مشاهده نشد.
پس از انجام اين آزمايشات، دانشمندان شرکت Triton به استفاده از پادتن anti-Ep-CAM روي آوردند و توانستند فرآيند ساخت نانوذرات مغناطيسي را بهبود داده و ذراتي توليد كنند كه هفت برابر بيشتر از نانوذرات قبلي گرما توليد كنند. اين شركت شروع آزمايشات باليني بر روي انسان را با استفاده از نانوذرات مغناطيسي متصل به پادتن anti-Ep-CAM؛ درسال 2006 تخمين زد.
اين كار مطالعاتي در دو مقاله با عناوين
"Development of tumor targeting bioprobes (¹¹¹In-chimeric L6 monoclonal Antibody nanoparticles) for alternating magnetic field Cancer therapy,"
"Application of high amplitude alternating magnetic fields for Heat induction of nanoparticles localized in cancer."
به تفصيل شرح داده شده است.
استفاده از نانولولههاي کربني در حرارتدرماني سرطان
گروهي از محققان مرکز پزشکي Baptist در دانشگاه Wake Forest روشي براي درمان سرطان با استفاده از نور ليزر يافتهاند. در اين روش نور ليزر نانوذرات را گرم کرده و حرارت ايجاد شده تومور را از بين ميبرد. آنها براي اين کار از نانولولههاي کربني چندديواره حاوي آهن استفاده کردهاند.
اين گروه تحقيقاتي در بررسيهاي آزمايشگاهي خود نشان دادهاند که ميتوانند با استفاده از يک روبشگر MRI، از اين نانوذرات درون بافتهاي زنده تصويربرداري کرده و رسيدن آنها به تومور و از بين بردن تومور را تماشا کنند.
با وجودي که اين کار بيشتر شبيه داستانهاي علمي-تخيلي است، اما کاملاً کاربردي و عملي است. اين کار بر يکي از روشهاي درمان سرطان به نام حرارتدرماني القاشده توسط ليزر (LITT) استوار است که از نور ليزر براي گرم کردن و از بين بردن تومورها بهره ميبرد. LITT بر اين واقعيت استوار است که برخي ذرات همچون نانولولههاي کربني چندديواره ميتوانند انرژي ليزر را جذب کرده و آن را به گرما تبديل کنند. اگر اين نانوذرات درون تومور گرم شوند، تومور را سوزانده و از بين ميبرند.
با اين حال مشکل LITT اين است که با وجودي که امکان مشاهده تومور در روبشهاي پزشکي وجود دارد، نانوذرات در اين روبشها ديده نميشوند. اگر نانوذرات را درون بدن بيمار تزريق نماييم، امکان ردگيري آنها وجود ندارد و اين امر ميتواند براي بيمار خطرناک باشد. زيرا اگر اين ذرات درون بافتهاي سالم تجمع نمايند، گرم کردن آنها ميتواند به از بين رفتن اين بافتها بيانجامد.
حال محققان دانشگاه Wake Forest براي اولين بار نشان دادهاند که ميتوان نانوذراتِ قابل مشاهده در MRI توليد نموده و بدين ترتيب تصويربرداري و گرم کردن تومور را به طور همزمان انجام داد. با پُر کردن نانولولههاي کربني چندديواره با آهن ميتوان آنها را با روبشگر MRI مشاهده کرد. آنها با استفاده از بافتهاي حاوي تومور موش نشان دادند که اين نانولولههاي حاوي آهن ميتوانند با بهرهگيري از تابش ليزر تومورها را از بين ببرند.
ژوآن فنگ دينگ، يکي از پژوهشگران اين کار ميگويد: «يافتن محل دقيق نانوذرات در بدن انسان براي درمان بسيار مهم است. ديدن اينکه تومورهاي نشاندار شده با نانولولهها بعد از درمان کوچکتر شدهاند، بسيار هيجانانگيز است».
اگر ثابت شود که اين روش مفيد است، شايد روزي به درمان بيماران سرطاني کمک کند، اما قبل از آن بايد کارايي اين روش در بررسيهاي باليني به اثبات برسد.
نتايج اين تحقيق در پنجاه و دومين همايش سالانه American Association of Physicists in Medicine در فيلادلفيا ارائه شده است.