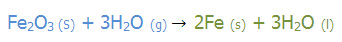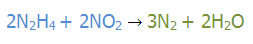موازنه کردن به روش وارسی
رایج ترین روش برای موازنه کردن یک معادله شمیایی، روش وارسی نام دارد. در این روش
ابتدا لازم است برای برابر کردن تعداد اتم های هر یک از عنصرها در دو سوی معادله، عنصر به عنصر مراحل انتخاب ضریب (برای یک واکنش دهنده ها یا فراورده دارای آن عنصر) صورت پذیرد و سپس اقدام به شمارش اتم ها در دو سوی معادله کرد.
برای موازنه کردن معادله ی شیمیایی واکنش به روش وارسی اقدامات زیر الزامی است:
-
1- تعداد اتم های هر یک از عنصرها در دو طرف واکنش شمرده شود.
-
2- انتخاب عنصر مرجع:
-
یک ترکیب از واکنش دهنده ها یا فراورده یا بیش ترین تعداد اتم از عنصری غیر از هیدروژن و اکسیژن انتخاب شود و برای آن اتم موازنه برای دو طرف معادله انجام شود.
-
3- تعداد اتم های اکسیژن موازنه گردد.
-
4- در پایان تعداد اتم های هیدروژن نیز موازنه گردد.
انتخاب عنصر آغاز گر برای موازنه، حساس ترین مرحله در موازنه یک واکنش شیمیایی است.
این عنصر باید به ترتیب اولویت شرایط زیر را داشته باشد:
-
1- در هر سمت واکنش فقط در ساختار یک ماده حضور داشته باشد.
-
2- تا حد امکان نباید در ساختار یک ماده ی تک عنصری شرکت داشته باشد، مگر این که هیچ عنصری شرط اول را نداشته باشد.
-
3- بین دو عنصر که هر دو شرایط 1 و 2 را دارند موازنه را از ساختار ترکیبی آغاز می کنیم که نوع و تعداد اتم های بیشتر باشد.
-
4- اگر بین دو عنصر، شرایط بالا یکسان بود، به زیر وند ها دقت می کنیم و ابتدا عنصری را موازنه می کنیم که زیر وند بزرگتری دارد.
نکته: اگر در موازنه با ضریب کسری مواجه شدیم، کل طرفین را باید در کوچکترین مضرب مشترک کسرها ضرب کنیم تا ضریب های کسری از بین بروند.
به مثال های زیر توجه کنید:
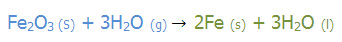
عنصر آغازگر Fe است.
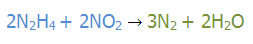
عنصر آغاز گر H است.